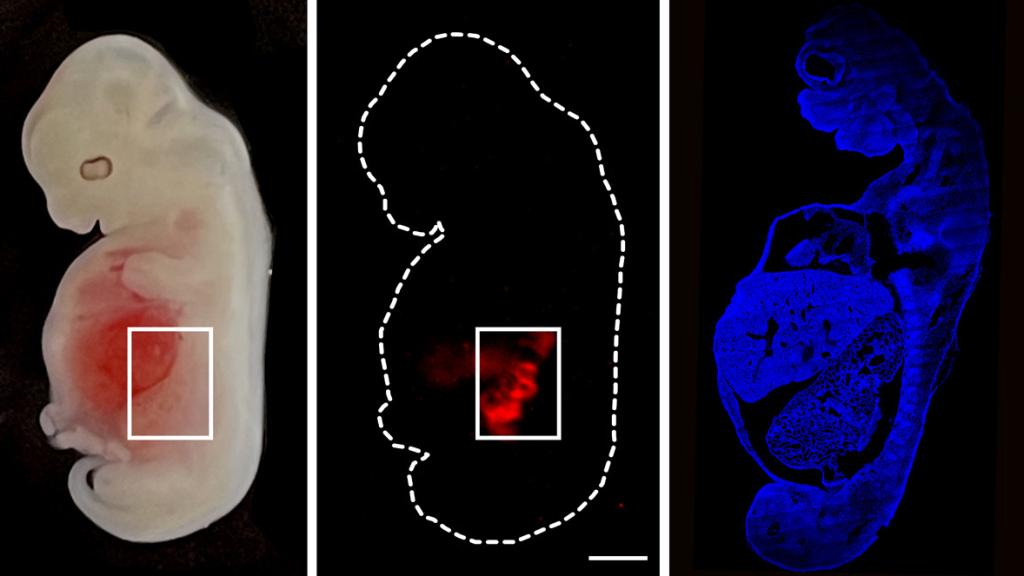
En rojo, las células humanizadas de riñón en el embrión de cerdo. Cell Stem Cell
Cultivan por primera vez riñones humanos en embriones de cerdo de hasta 28 días
El paso dado acerca la posibilidad de generar órganos para trasplante en animales no humanos, si bien los autores reconocen que falta mucho por hacer.
Un equipo de investigadores de los Institutos Guangzhou de Biomedicina y Salud, en China, han logrado hacer crecer riñones humanizados en embriones de cerdo. Se trata de una prueba de concepto que marca un antes y un después en la posibilidad –lejana, de momento– de cultivar órganos humanos en animales para utilizarlos posteriormente en trasplantes.
A diferencia de los trasplantes de órganos de cerdo realizados de forma experimental en los últimos años, no se trata de suprimir ciertos genes para evitar el rechazo inmediato por parte del cuerpo humano.
En esta ocasión, los científicos han introducido células madre pluripotentes humanas en embriones de cerdo, que darán lugar a unos riñones que se podrían considerar humanos: entre el 50% y el 60% de las células que conformaban su estructura procedían de estas células madre humanas.
[La edad dorada de los trasplantes de órganos: "Hemos hecho rutinario algo de ciencia ficción"]
Transfirieron 1.820 embriones quiméricos (híbridos cerdo-humano) en 13 cerdas, que los gestaron durante un periodo de entre 25 y 28 días. Tras este lapso de tiempo, los extrajeron y analizaron cinco de ellos para comprobar cómo las células se habían ido distribuyendo.
Aquí tenían que superar un problema. Un embrión procede de una única célula (producto de la unión de un óvulo y un espermatozoide) que se va dividiendo. A medida que lo hace, las células resultantes se van diferenciando del resto para generar tejidos específicos.
Para generar riñones humanos, había que evitar que las células embrionarias del cerdo se diferenciaran hacia esa dirección. Desactivando dos genes mediante la tecnología CRISPR, los investigadores crearon un 'nicho' para que las células humanas pudieran desarrollarse con normalidad en un entorno que no era el suyo.
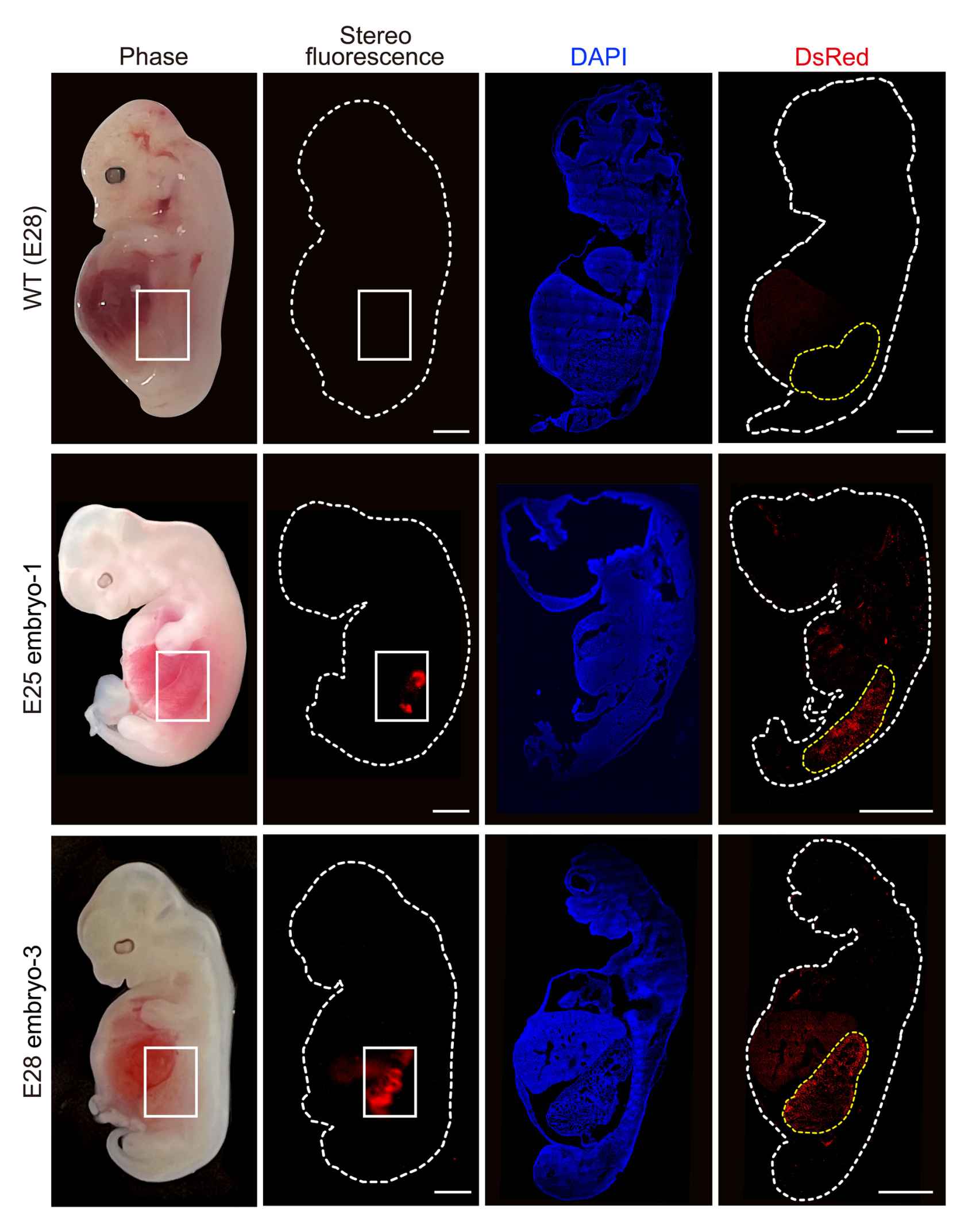
En rojo se ven las células renales humanizadas desarrollándose en el embrión. Cell Stem Cell
Entonces surge otro problema, quizá el más delicado desde una perspectiva ética. Al tratarse de células madre pluripotentes humanas, cabía la posibilidad de que, división tras división, comenzaran a migrar a otras partes del embrión y diferenciarse en otro tipo de tejidos.
El principal peligro es que las células humanas acabaran en tejidos neurales o de la línea germinal. Es decir, que el embrión, de desarrollarse plenamente, tuviera un sistema nervioso humanizado, o que su sistema reproductor lo fuera, transfiriendo información humana a su potencial prole.
Un cerebro porcino 'humanizado'
En el artículo en que han dado a conocer el experimento, publicado este jueves en la revista Cell Stem Cell, los científicos explican que los riñones de los embriones eran estructuralmente normales para su etapa de desarrollo, habían formado túbulos y brotes de células que acabarían siendo los conductos que los conectan con la vejiga. En general había entre un 50% y un 60% de células humanas en ellos.
Además, hallaron muy pocas células humanas en el cerebro y la espina dorsal de los embriones "y ninguna en la cresta genital [que dará lugar a los órganos reproductores], indicando que las células madre pluripotentes humanas no se diferencia en células germinales", apunta Zhen Dai, uno de los autores.
La perspectiva ética es la más delicada en este tipo de experimentos. No en vano, se ha realizado en China, donde hay más laxitud en este campo. De hecho, el investigador español Juan Carlos Izpisúa trasladó a su equipo al país oriental para lograr embriones híbridos de humano y primate en 2019, cortando el experimento a las 14 semanas, ya que ese es el momento en que comienza a desarrollarse el sistema nervioso central.
[El corazón de cerdo que fue trasplantado por primera vez a un hombre tenía un virus]
Antes, había hibridado ratones y ratas, para que estas desarrollaran órganos de ratón, y había creado embriones quiméricos cerdo-humano, aunque no se desarrolló ningún órgano humanizado, ya que el objetivo era demostrar la posibilidad de la hibridación. Con todo, el experimento se detuvo a las tres semanas, límite legal en Europa para estas investigaciones.
En declaraciones al Science Media Centre, el fundador y exdirector de la Organización Nacional de Trasplantes, Rafael Matesanz, explica que la técnica utilizada por el equipo chino "aumentó en gran medida la eficiencia del procedimiento, que era uno de los puntos débiles de estos experimentos".
Los investigadores reconocen que queda mucho por hacer antes de crear unos riñones plenamente viables. Por ejemplo, las células vasculares (las que crean los vasos sanguíneos) de los embriones eran de cerdo, lo que podría causar rechazo en un hipotético trasplante.
[Matesanz: "¿Cómo se le ofrece un corazón de cerdo a alguien que podría recibir uno humano?"]
No obstante, quieren seguir avanzando, dejando crecer más los embriones y probando con otros órganos candidatos a trasplante, como el corazón y el páncreas (el riñón es el órgano más trasplantado en todo el mundo).
De momento, este avance y los próximos que vengan ayudarán a comprender la formación de los órganos en el desarrollo embrionario, cómo a partir de unas pocas células se van generando tejidos completamente distintos, cada uno en su sitio, y logran un cuerpo completo.
"Los propios autores reconocen que para el uso clínico de esta tecnología faltan años", continúa Matesanz, "pero se trata de un logro muy importante en el camino de lograr una producción ilimitada de órganos para trasplante".




