Administrando un inyectable contra el VIH.
El Gobierno da luz verde a la financiación de la PrEP inyectable frente al VIH que se administra cada dos meses
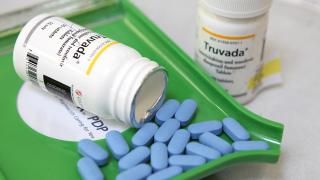
Se trata de Apretude, un fármaco de ViiV Healthcare y se financiará en situaciones en las que la pastilla oral no funcione.
Más información: Del estigma de la enfermedad al de la promiscuidad: cinco años de la píldora que nos hizo perder el miedo al VIH
Luz verde a la primera profilaxis pre-exposición (conocida como PrEP) inyectable frente al VIH en la sanidad pública. La Comisión Interministerial de Precios de los Medicamentos (CIPM) ha acordado la financiación pública de este fármaco subcutáneo comercializado por ViiV Healthcare y más conocido como Apretude (cabotegravir de acción prolongada).
Esta aprobación convierte a España en el primer país de la Unión Europea (UE) en incluir esta innovación terapéutica en la cartera de servicios de su sistema nacional de salud.
La decisión adoptada en el seno del órgano competente en materia de financiación y fijación de precios de medicamentos garantiza su incorporación como prestación farmacéutica del sistema público.
Apretude está indicado para personas VIH negativas con alto riesgo de adquirir la infección por vía sexual. Su administración intramuscular, cada dos meses, elimina la necesidad de una toma diaria, como ocurre con la PrEP oral.
De esta forma, facilita la adherencia en determinados perfiles de población.
Los ensayos clínicos internacionales han demostrado que el cabotegravir de acción prolongada ofrece una elevada eficacia en la prevención de la infección por VIH en comparación con la pauta oral diaria en contextos donde la adherencia puede verse comprometida.
La autorización para su comercialización fue concedida por la Agencia Europea de Medicamentos (EMA), permitiendo su disponibilidad en los Estados miembros. Con esta decisión de financiación pública, España se sitúa a la vanguardia europea en la incorporación de innovaciones preventivas frente al VIH.
La medida se alinea con las recomendaciones de la Organización Mundial de la Salud (OMS) y de Onusida, que instan a ampliar el acceso a estrategias de prevención eficaces para avanzar hacia la eliminación de esta enfermedad como problema de salud pública.